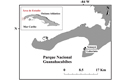
Relación de la densidad e intensidad de pastoreo de los peces herbívoros (Scaridae y Acanthuridae) con las macroalgas en el Occidente de Cuba
##plugins.themes.bootstrap3.article.main##
Resumen
Los peces de las familias Scaridae y Acanthuridae son herbívoros que controlan el crecimiento algal sobre los corales. Su exclusión por la pesca ilícita y el desarrollo costero conduce rápidamente al dominio de las macroalgas en el arrecife. Para estimar la densidad e intensidad de pastoreo de Scaridae y Acanthuridae y su relación con la cobertura de macroalgas, se seleccionaron dos veriles en el Parque Nacional Guanahacabibes (PNG) y uno en La Habana (LH), este último con elevada degradación antrópica. Se usaron video-cuadrantes de 1 m2 para obtener la densidad de peces (individuos/m2) e intensidad de pastoreo (mordidas/5 minutos*m2) y cuadrantes de 25x25 cm para la abundancia relativa de macroalgas. Se identificaron diez especies, Scaridae predominó en el PNG y Acanthuridae en LH. La pérdida de Scaridae en LH, implica que Acanthuridae representa un exceso de un grupo funcional que no provee el sustrato desnudo para el reclutamiento coralino. Hubo fuerte correlación positiva entre la densidad e intensidad de pastoreo de Scaridae con Halimeda, dado que en el PNG esta alga se favorece y constituye un alimento recurrente y eficiente para Scaridae. En LH predominaron algas bioindicadoras de eutrofización como Stypopodium y sólo mostró correlación positiva con Acanthuridae. Estos peces consumen las epífitas sobre Stypopodium, y sus tasas de pastoreo son más altas, lo cual contribuye al cultivo de algas cespitosas, fuertes competidoras del espacio con los corales. De ahí la importancia de presentar comunidades más equitativas con diferentes grupos funcionales de peces herbívoros que contribuyan a un control más efectivo de las macroalgas.
##plugins.themes.bootstrap3.article.details##
herbivorismo, arrecife, Parque Nacional Guanahacabibes, sobrepesca
Atlantic and Gulf Rapid Reef Assessment (AGRRA). 2001. The AGRRA Rapid Assessment Protocol. Atlantic and gulf Rapid Reef Assessment methodology. http://coral.aoml.noaa.gov/agra/methodhome.htm (accesado: junio 25, 2001).
Aguilar, C. 2005. Ictiofauna costera de Ciudad de la Habana, efectos acumulativos de agentes estresantes múltiples en varios niveles de organización biológica. Tesis en opción al grado científico de Doctora en Ciencias Biológicas, 122 pp.
Arias-González, J. E., T. Fung, R. Seymour, J. Garza-Pérez, G. Acosta-González, Y. Bozec y C. Jhonson. 2017. A coral–algal phase shift in Mesoamerica not driven by changes in herbi vorous fish abundance. PLoS ONE, 12 (4). https://doi.org/10.1371/journal.pone.0174855
Ávila-Alonso, D., M. Guimaraes y R. Cárdenas. 2013. Variación espacio-temporal de grupos morfo-funcionales de macroalgas en pastos marinos al norte de Ciego de Ávila, Cuba. Revista de Investigaciones Marinas, 33 (1): 14–22. ISSN: 1991–6089.
Burkepile, D. E. 2012. Context-dependent corallivory by parrotfishes in a Caribbean reef ecosystem. Coral Reefs, 31 (1): 111–120. https://doi.org/10.1007/s00338-011-0824-5
Burkepile, D. E. y M. E. Hay. 2011. Feeding complementarity versus redundancy among herbivorous fishes on a Caribbean reef. Coral Reefs, 30 (2): 351–362. https://doi.org/10.1007/s00338-011-0726-6
Cabrera-Guerra, D., P. Chevalier-Monteagudo, D. Cobián, R. Corrada, R. Fernández, H. Caballero y K. Campos. 2018. Variación espacio-temporal de los peces herbívoros (Acanthuridae y Scaridae) en dos localidades arrecifales de Cuba con diferentes niveles de conservación. Revista de Investigaciones Marinas, 38: 67–82. ISSN:1991–6086 RNPS:2096
Castellanos-Gell, J., A. Robainas-Barcia, D. Casane, P. Chevalier-Monteagudo, F. Pina-Amargós y E. García-Machado. 2012. The surgeonfish, Acanthurus bahianus, has crossed the Amazon-Orinoco outflow barrier. Marine Biology, 159: 1561–1565. https://doi.org/10.1007/s00227-012-1942-5
Castro-Sanguino, C., C. Lovelock y P. J. Mumby. 2016. The effect of structurally complex corals and herbivory on the dynamics of Halimeda. Coral Reefs, 35: 597–606. https://doi.org/10.1007/s00338-016-1412-5
Cheal, A. J., M. A. MacNeil, E. Cripps, M. J. Emslie, M. Jonker, B. Schaffelke y H. Sweatman. 2010. Coral–macroalgal phase shifts or reef resilience: links with diversity and functional roles of herbivorous fishes on the Great Barrier Reef. Coral Reefs, 29 (4): 1005–1015. https://doi.org/10.1007/s00338-010-0661-y
Claro, R. y J. García-Arteaga. 2001. Growth patterns of fishes of the Cuban shelf, (pp. 149–178). En: Claro R., K. C. Lindeman y L. R. Parenti (Eds.). Ecology of the marine fishes of Cuba, Smithsonian Institution Press, Washington y Londres, 270 pp.
Claro, R. y K. Cantelar Ramos. 2003. Rapid assessment of coral communities of María la Gorda, southeast Ensenada de Corrientes, Cuba (Part 2: Reef fishes). Atoll Research Bulletin, 496 (16): 278–293. https://doi.org/10.5479/si.00775630.496-16.278
Cobián-Rojas, D. 2016. Impacto potencial del pez león sobre la comunidad de peces en dos áreas marinas protegidas del Caribe (Cuba y México). Tesis presentada como requisito parcial para optar al grado de Doctorado en Ciencias en Ecología y Desarrollo Sustentable Con orientación en Conservación de la Biodiversidad, 126 pp.
Cobián-Rojas, D., R. Claro, P. Chevalier-Monteagudo, S. Perera y H. Caballero. 2011. Estructura de las asociaciones de peces en los arrecifes coralinos del Parque Nacional Guanahacabibes, Cuba. Revista Marina y Costera, 3: 153–169. https://doi.org/10.15359/revmar.1.6
Cronin, G., V. J. Paul, M. E. Hay y W. Fenical. 1997. Are tropical herbivores more resistant than temperate herbivores to seaweed chemical defenses? Diterpenoid metobolites from Dictyota acutiloba as feeding deterrents for tropical versus temperate fishes and urchins. Journal of Chemical Ecology, 23 (2): 289–302. https://doi.org/10.1023/B:JOEC.0000006360.36833.13
Delfín, S. 2018. Diversidad de organismos herbívoros en dos crestas arrecifales de la región noroccidental de Cuba. Tesis presentada en opción al título de Licenciado en Biología, Universidad de la Habana, Cuba, 106 pp.
Den Haan, J., J. Huisman, F. Dekker, J. ten Brinke, A. K. Ford, J. van Ooijen, F. van Duyl, M. Vermeij y P. M. Visser. 2013. Fast detection of nutrient limitation in macroalgae and seagrass with nutrient–induced fuorescence. PLoS ONE, 8 (7). https://doi.org/10.1371/ journal.pone.0068834
Duran, A. y R. Claro. 2009. Actividad alimentaria de los peces herbívoros y su impacto en arrecifes con diferente nivel de degradación antrópica. Revista de Biología Tropical, 57 (3): 687–697.
Duran, A., A. A. Shantz, D. E. Burkepile, L. Collado-Vides, V. M. Ferrer, L. Palma, A. Ramos y P. González-Díaz. 2018. Fishing, pollution, climate change, and the long term decline of coral reefs off Havana, Cuba. Bulletin of Marine Science, 94 (2): 213–228. https://doi.org/10.5343/bms.2017.1061
Edwards, C. B., A. M. Friedlander, A. G. Green, M. J. Hardt, E. Sala, H. P. Sweatman, I. Williams, B. Zgliczynski, A. Sandin y J. E. Smith. 2014. Global assessment of the status of coral reef herbivorous fishes: evidence for fishing effects. Proceedings of the Royal Society B: Biological Sciences, 281(1774). https://doi.org/10.1098/rspb.2013.1835
Ferreira, C. E. y J. E. A. Gonçalves. 2006. Community structure and diet of roving herbivorous reef fishes in the Abrolhos Archipelago, south?western Atlantic. Journal of Fish Biology, 69 (5): 1533–1551. https://doi.org/10.1111/j.1095-8649.2006.01220.x
Fox, R. J. y D. R. Bellwood. 2007. Quantifying herbivory across a coral reef depth gradient. Marine Ecology Progress Series, 339: 49–59.
Francini-Filho, R. B., C. M. Ferreira, E. O. C. Coni, R. L. De Moura y L. Kaufman. 2010. Foraging activity of roving herbivorous reef fish (Acanthuridae and Scaridae) in eastern Brazil: influence of resource availability and interference competition. Journal of the Marine Biological Association UK, 90 (3): 481–492. https://doi.org/10.1017/S0025315409991147
Froese, R. y D. Pauly. 2019. FishBase. World Wide Web electronic publication. www.fishbase.org, version 06/2017.
García-Rodríguez, A., A. L. Lorenzo y N. G. Rodríguez. 2012. Evaluación de las asociaciones de peces arrecifales en el oeste del litoral de La Habana, zona noroccidental de Cuba. Serie Oceanológica, 11: 77–90.
González-Sansón, G. y C. Aguilar. 2010. Reef fish diversity components as indicators of cumulative effects in a highly impacted fringe reef. Ecological Indicators, 10: 766–772. https://doi.org/10.1016/j.ecolind.2009.11.009
Green, A. L. y D. R. Bellwood. 2009. Monitoring functional groups of herbivorous reef fishes as indicators of coral reef resilience – A practical guide for coral reef managers in the Asia Pacific region. IUCN working group on Climate Change and Coral Reefs. IUCN, Gland, Switzerland, 70 pp.
Hawkins, J. P. y C. M. Roberts. 2003. Effects of fishing on sex–changing Caribbean parrotfishes. Biological Conservation, 115: 213–226. https://doi.org/10.1016/S0006-3207(03)00119-8
Hernández?Landa, R. C., G. Acosta?González, E. Núñez?Lara y J. E. Arias?González. 2014. Spatial distribution of surgeonfish and parrotfish in the north sector of the Mesoamerican Barrier Reef System. Marine Ecology, 36 (3): 432–446. https://doi.org/10.1111/maec.12152
Hoey, A. S. y D. R. Bellwood. 2010. Among–habitat variation in herbivory on Sargassum spp. on a mid-shelf reef in the northern Great Barrier. Reef. Marine Biology, 157 (1): 189–200. https://doi.org/10.1007/s00227-009-1309-8
Human, P. y N. DeLoach. 2014. Reef fish identification. Florida, Caribbean, Bahamas. (4th, Ed): New World Publications, Inc, Florida, Estados Unidos, 537 pp.
Iturralde-Vinent, M. 2010. Geología de Cuba para todos. Editorial Científico-Técnica, La Habana, Cuba, 150 pp.
Jackson, J., M. Donovan, K. Cramer y V. Lam. (Eds). 2014. Status and Trends of Caribbean Coral Reefs: 1970–2012. Global Coral Reef Monitoring Network. IUCN, Gland, Switzerland, 304 pp.
Kopp, D., Y. Bouchon-Navaro, M. Louis, P. Legendre y C. Bouchon. 2012. Spatial and Temporal Variation in a Caribbean Herbivorous Fish Assemblage. Journal of Coastal Research, 28 (1A): 63–72. https://doi.org/10.2112/JCOASTRES-D-09-00165.1
Lewis, S. M. 1985. Herbivory on coral reefs: algal susceptibility to herbivorous fishes. Oecologia, 65 (3): 370–375. https://doi.org/10.1007/BF00378911
Littler, M. M. y D. S. Littler. 1984. Relationships between macoalgal functional form groups and substrata stability in a subtropical rocky-intertidal system. Journal of Experimental Marine Biology and Ecology, 74 (1): 13–34. https://doi.org/10.1016/0022-0981(84)90035-2
Loffler, Z., A. Graba-Landry, J. T. Kidgell, E. McClure, M. S. Pratchett y A. S. Hoey. 2018. Holdfasts of Sargassum swartzii are resistant to herbivory and resilient to damage. Coral Reefs, 37 (4): 1075–1084. https://doi.org/10.1007/s00338-018-01745-w
Luna-Ortega, I. y F. de la Cruz. 2017. Ensambles de macroalgas sobre superficies muertas de corales escleractíneos (Anthozoa: Scleractinea) en el arrecife Oro Verde, Veracruz, México. Oceánides, 32 (1): 11–23. http://dx.doi.org/10.37543/oceanides.v32i1.192
Marshell, A. y P. J. Mumby. 2015. The role of surgeon?sh (Acanthuridae) in maintaining algal turf biomass on coral reefs. Journal of Experimental Marine Biology and Ecology, 473: 152–160. https://doi.org/10.1016/j.jembe.2015.09.002
Mumby, P. J. 2016. Stratifying herbivore fisheries by habitat to avoid ecosystem overfishing of coral reefs. Fish and Fisheries, 17 (1): 266–278. https://doi.org/10.1111/faf.12078
Mumby, P. J., J. Flower, I. Chollett, J. S. Box, Y. M. Bozec, C. Fitzsimmons, …y S. M. Williams. 2014. Hacia la resiliencia del arrecife y medios de vida sustentables: Un manual para los administradores de arrecifes de coral del Caribe. Exeter: University of Exeter, 172 pp.
Olivares-Rieumont, S., D. de la Lanza, L. Lima, D.W. Graham, K. D´Alessandro, J. Borroto, F. Martínez y J. Sánchez. 2005. Assessment of heavy metal levels in Almendares River sediments Havana City, Cuba. Water Research, 39: 3945–3953. https://doi.org/ 10.1016/j.watres.2005.07.011
Östman, Ö., J. Eklöf, B. K. Eriksson, J. Olsson, P. O. Moksnes y U. Bergström. 2016. Top?down control as important as nutrient enrichment for eutrophication effects in North Atlantic coastal ecosystems. Journal of Applied Ecology, 53 (4): 1138–1147. https://doi.org/ 10.1111/1365-2664.12654
Perera-Valderrama, S., H. Hernández-Arana, M. Á. Ruiz-Zárate, P. M. Alcolado, H. Caballero-Aragón, J. González-Cano, J. González-Cano y D. Cobián-Rojas. 2016. Condition assessment of coral reefs of two marine protected areas under different regimes of use in the north-western Caribbean. Ocean & Coastal Management, 127: 16–25. https://doi.org/ 10.1016/j.ocecoaman.2016.04.001
Perera-Valderrama, S., H. Hernández-Arana, M. Á. Ruiz-Zárate, P. M. Alcolado, H. Caballero-Aragón, J. González-Cano, ... y E. de la Guardia-Llansó. 2017. Temporal dynamic of reef benthic communities in two marine protected areas in the Caribbean. Journal of Sea Research, 128: 15–24. https://doi.org/10.1016/j.seares.2017.07.007
Santana-Romero, J. L., M. Valdés-Callado, S. Olivares-Rieumont y L. Lima-Cazorla. 2012. Determinación de hidrocarburos aromáticos policíclicos ligeros en aguas superficiales de los ríos Almendares y Luyanó en La Habana. Revista CENIC. Ciencias Químicas, 43: 1–7.
Schutte, V. G., E. R. Selig y J. F. Bruno. 2010. Regional spatio–temporal trends in Caribbean coral reef benthic communities. Marine Ecology Progress Series, 402: 115–122. https://doi.org/10.3354/meps08438
Steneck, R. S. 1983. Quantifying herbivory on coral reefs: Just scratching the surface and still biting off more than we can chew. En L. Reaka (ed.): The ecology of deep and shallow coral reefs, Simposia Series for Undersea Reserarch. NOAA´SUndersea Research Program, 1 (1): 103–111.
Steneck, R. S. y M. N. Dethier. 1994. A functional group approach to the structure of algal-dominated communities. Oikos, 69: 476–498. https://doi.org/10.2307/3545860
Suárez, A. M., B. Martínez-Daranas y Y. Alfonso. 2014. Macroalgas marinas de Cuba. Universidad de la Habana, 262 pp.
Taylor, B. M., S. J. Lindfield y J. H. Choat. 2015. Hierarchical and scale-dependent effects of fishing pressure and environment on the structure and size distribution of parrotfish communities. Ecography, 38 (5): 520–530. https://doi.org/10.1111/ecog.01093
Toller, W., A. O. Debrot, M. J. Vermeij y P. C. Hoetjes. 2010. Reef fishes of Saba Bank, Netherlands Antilles: assemblage structure across a gradient of habitat types. PloS ONE, 5 (5). https://doi.org/10.1371/journal.pone.0009207
Vergés, A., C. Doropoulos, H. A. Malcolm, M. Skye, M. Garcia-Pizá, E. M. Marzinelli... y P. D. Steinberg. 2016. Long–term empirical evidence of ocean warming leading to tropicalization of fish communities, increased herbivory, and loss of kelp. Proceedings of the National Academy of Sciences, 113 (48): 13791–13796. https://doi.org/10.1073/pnas.1610725113
Vermeij, M. J., I. Van Moorselaar, S. Engelhard, C. Hornlein, S. M. Vonk y P. M. Visser. 2010. The effects of nutrient enrichment and herbivore abundance on the ability of turf algae to overgrow coral in the Caribbean. PLoS ONE, 5 (12): e14312 https://doi.org/10.1371/journal.pone.0014312
Welsh, J. Q., R. M. Bonaldo y D. M. Bellwood. 2015. Clustered parrotfish feeding scars trigger partial coral mortality of massive Porites colonies on the inshore Great Barrier Reef. Coral Reefs, 34 (1): 81–86. https://doi.org/10.1007/s00338-014-1224-4

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial 4.0.
Cómo citar
Métricas del artículo
- 807 Vistas Resumen vistas
- 446 Descargas PDF Descargas
- 137 Vistas Html Vistas